近日,南京试剂向国家食品药品监督管理总局药品审评中心(CDE)申报的首批药用辅料备案登记资料已经被受理,其中,三氯甲烷、醋酸钠、依地酸二钠等3个品种已通过完整性审查并在其官网平台公示。此外,盐酸、乙醇、尿素等多个品种正在审核过程中。
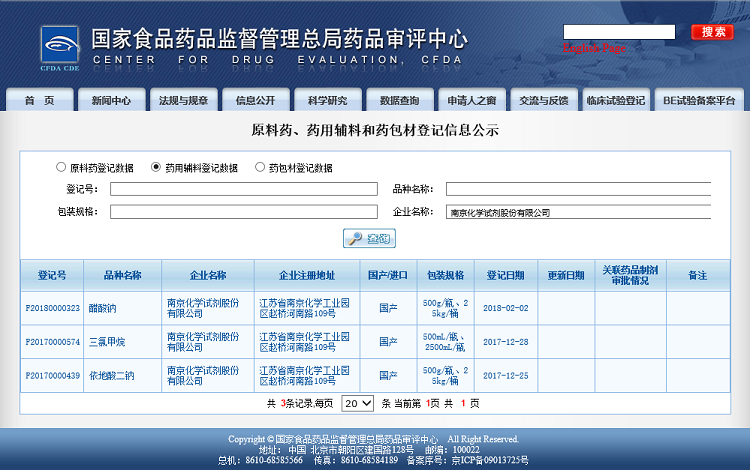
2016年8月,国家食品药品监督管理总局发布134号文件《关于药包材药用辅料与药品关联审评审批有关事项的公告》;2017年12月,又发布《原料药、药用辅料及药包材与药品制剂共同审评审批管理办法》(征求意见稿),药用辅料申报由批件制改为共同审评审批制。
随着关联审评的实施,公司药辅、研发和质检团队,加快对30个已经取得生产批件的药辅品种备案登记。同时,接受多家制药企业邀请,参与新药研制的共同审评资料申报,开展丙酮、磷酸、马来酸、叔丁醇、琥珀酸、乙二醇苯醚、苯甲酸苄酯等多种药辅产品工艺研究和质量研究。
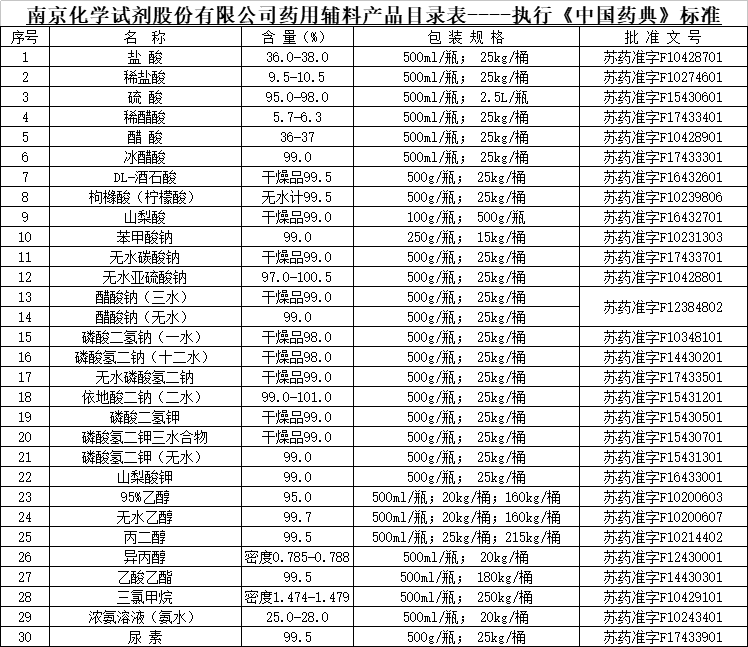
“十三五”期间,南京试剂把药辅作为发展战略重点,加大资源投入,先后建成10万级局部百级超净包装线、微生物实验室,参照GMP标准建设洁净车间、自动灌装线。同时,公司对接药企标准,完善药辅工艺技术、生产流程、过程控制、成品包装、储存运输等各个环节管理,不断提升产品质量,增强服务顾客的能力。

欢迎新老顾客和业界同仁来电垂询和探讨。
药辅部:025-85316064/65/66转3078
e-mail: rdm@nj-reagent.com。








 MSDS搜索
MSDS搜索 COA搜索
COA搜索 危险和安全代码
危险和安全代码 危害和防护代码
危害和防护代码 技术支持
技术支持 投诉建议
投诉建议 在线客服
在线客服